Ионный обмен — обратимый химический процесс между ионитом и компонентами раствора. В зависимости от заряда ионов, участвующих в реакции, различают катионный и анионный обмен.
Принцип и механизм ионообмена
В основе технологии лежит использование ионообменных материалов — ионитов (ионообменников). Чаще всего это полимерные смолы или волокнистый материал. Все иониты можно представить в виде каркаса с зафиксированными функциональными группами, способными к ионообмену.
Простым примером ионного обмена может служить реакция умягчения воды:
R-Na + Ca2+ <=> R2Ca + Na+
Процесс равновесный и подчиняется закону действующих масс. Прямая реакция сводится к умягчению, обратная — к регенерации ионита.
Если в процессе участвует некоторый постоянный объем воды, то через определенное время настанет равновесие между жидкостью и ионообменным материалом. Реакция окончится, но по ряду причин не все связываемые катионы или анионы окажутся на ионите. Этот эффект называется ионным проскоком. Он наблюдается тем сильнее, чем ниже ресурс ионообменника.
Наглядно зависимости равновесных концентраций ионов А и Б в растворе от их содержания в ионообменнике можно представить в виде графика ниже.
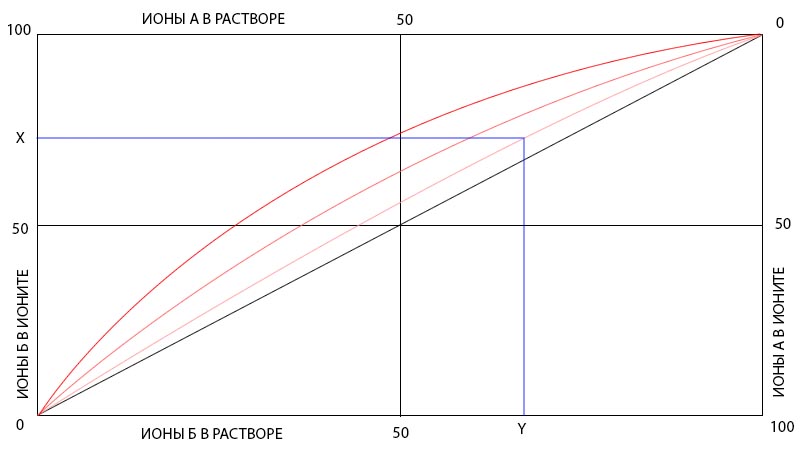
График позволяет увидеть, что в равновесном состоянии концентрация Y% компонента Б в жидкой фазе соответствует содержанию X% этого же компонента в ионите. Если ионы А и Б имеют одинаковое сродство к иониту, то кривая — диагональ прямоугольника. Чем сильнее смещается кривая вверх, тем более выражено предпочтение ионообменного материала в отношении иона Б.
Получается, что при участии в ионном обмене нескольких конкурирующих ионов, ионообменный материал будет связываться в большей степени с тем, кто имеет большее сродство с ним. Например, сульфополистирольная ионообменная смола при одинаковых концентрациях в воде ионов натрия и кальция будет связывать предпочтительно катионы кальция, что обусловлено большим сродством к Ca2+. Снижение концентрации раствора делает эту тенденцию еще более выраженной.
Насыщение ионита
Насыщение смолы ионами А можно наглядно отразить на кривой насыщения.
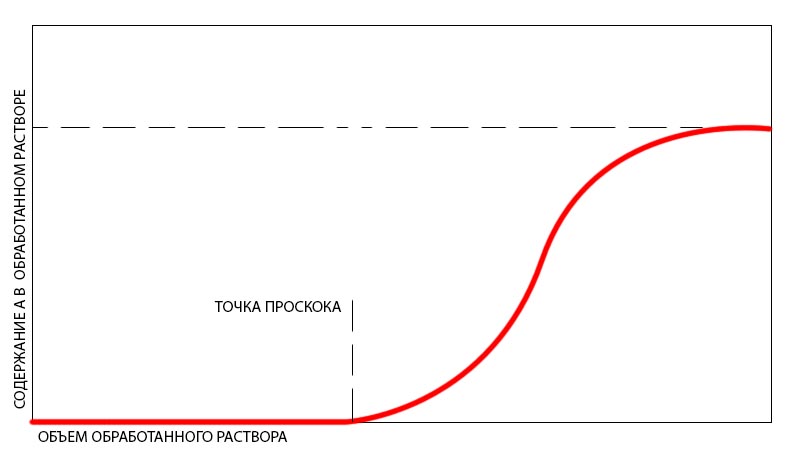
На процессы ионного обмена влияет несколько факторов:
- температура;
- концентрация ионов и их степень диссоциации;
- кинетика попадания ионов на ионит и внутрь его каркаса;
- характер взаимодействия ионита и раствора.
По этой причине понятие полной емкости ионита, отражающее теоретические возможности для обмена не имеют практического значения. При выборе той же ионообменной смолы обращайте внимание на полезную емкость, которая рассчитана с учетом кривых насыщения и смещения изохронных кривых.
В нашем каталоге представлены самые разнообразные ионообменные фильтрующие материалы для станций водоподготовки. Нашлось место и картриджам с ионообменной смолой — любых размеров и форм.
Если понадобится консультация, всегда можно спросить совета у наших специалистов в чате или по телефону.